工艺的操作成本很大程度上是由层析填料的成本驱动的,因此层析填料可使用的批次或循环次数(层析填料寿命)对生产成本的控制至关重要。
层析填料寿命研究的法规要求
各国监管部门出于对药品安全性和有效性的考量,其法规文件明确规定了对“层析填料的使用寿命及可接受限度”的要求。
Table 1. 层析填料寿命研究的法规指南要求

此外,2021年,PDA发布了技术报告60-3《工艺验证:生命周期方法 附件2:生物制药原料药生产》,报告中明确提出提高层析介质的相关验证是工艺验证的重要部分。
层析填料寿命衰减的影响因素
层析填料寿命研究策略
层析填料寿命研究策略必须能够完全反映商业化生产规模的性能,或者必须能体现与商业化生产规模之间的相关性。Table 2. 层析填料寿命研究策略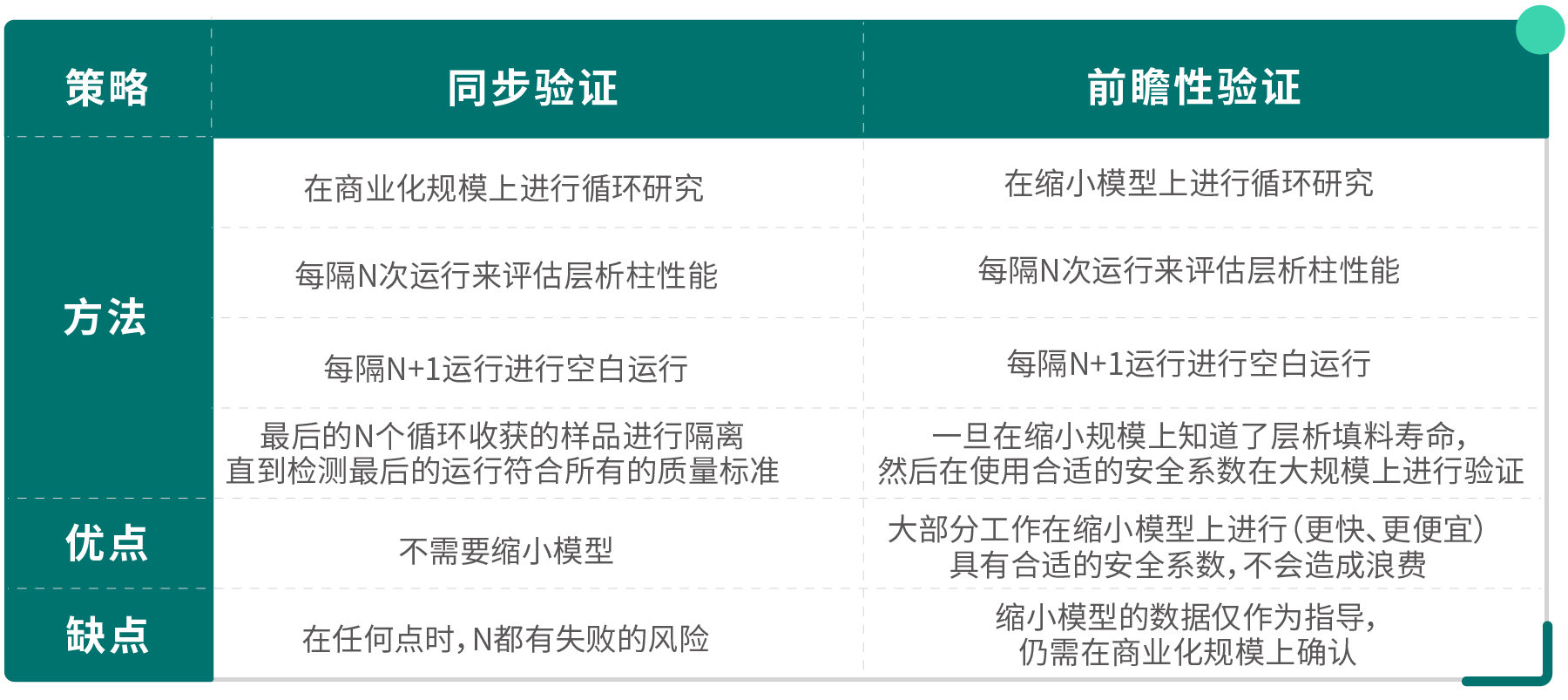 注:监控频率(N)可根据对工艺的理解和实际情况做适应性调整。
注:监控频率(N)可根据对工艺的理解和实际情况做适应性调整。
• 缩小模型(Scale Down)
• 空白运行(Carryover)
层析填料寿命研究的可接受标准
层析介质的使用寿命根据检测指标的标准来定义。检测指标的标准可以设定为一个具体的截止标准,比如收率>80%,SEC-HPLC 纯度>95%等,也可以通过检测循环次数间的一致性来定义,此时就不再设置具体数值标准。Table 3. 寿命研究的评价指标及其可接受标准(举例)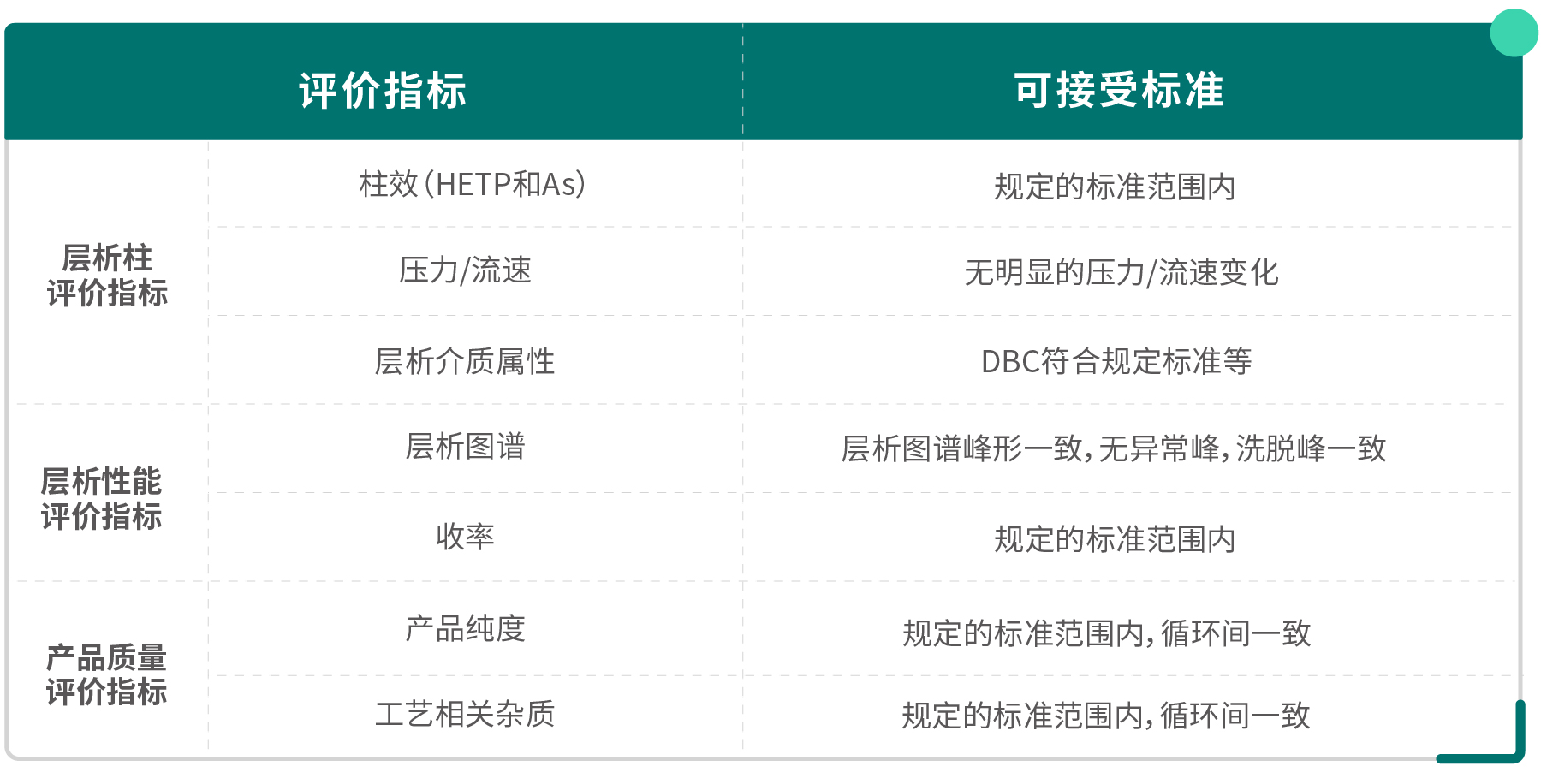 层析填料寿命研究的终点判定可以选择达到检测标准的循环次数数值,或者出现批间异常的循环次数数值。通常较为保守的做法是将确定的循环次数数值乘以一个安全系数,来定义最终的层析填料寿命次数。
层析填料寿命研究的终点判定可以选择达到检测标准的循环次数数值,或者出现批间异常的循环次数数值。通常较为保守的做法是将确定的循环次数数值乘以一个安全系数,来定义最终的层析填料寿命次数。
案例分享:博格隆抗体亲和填料Novo-A Diamond寿命研究
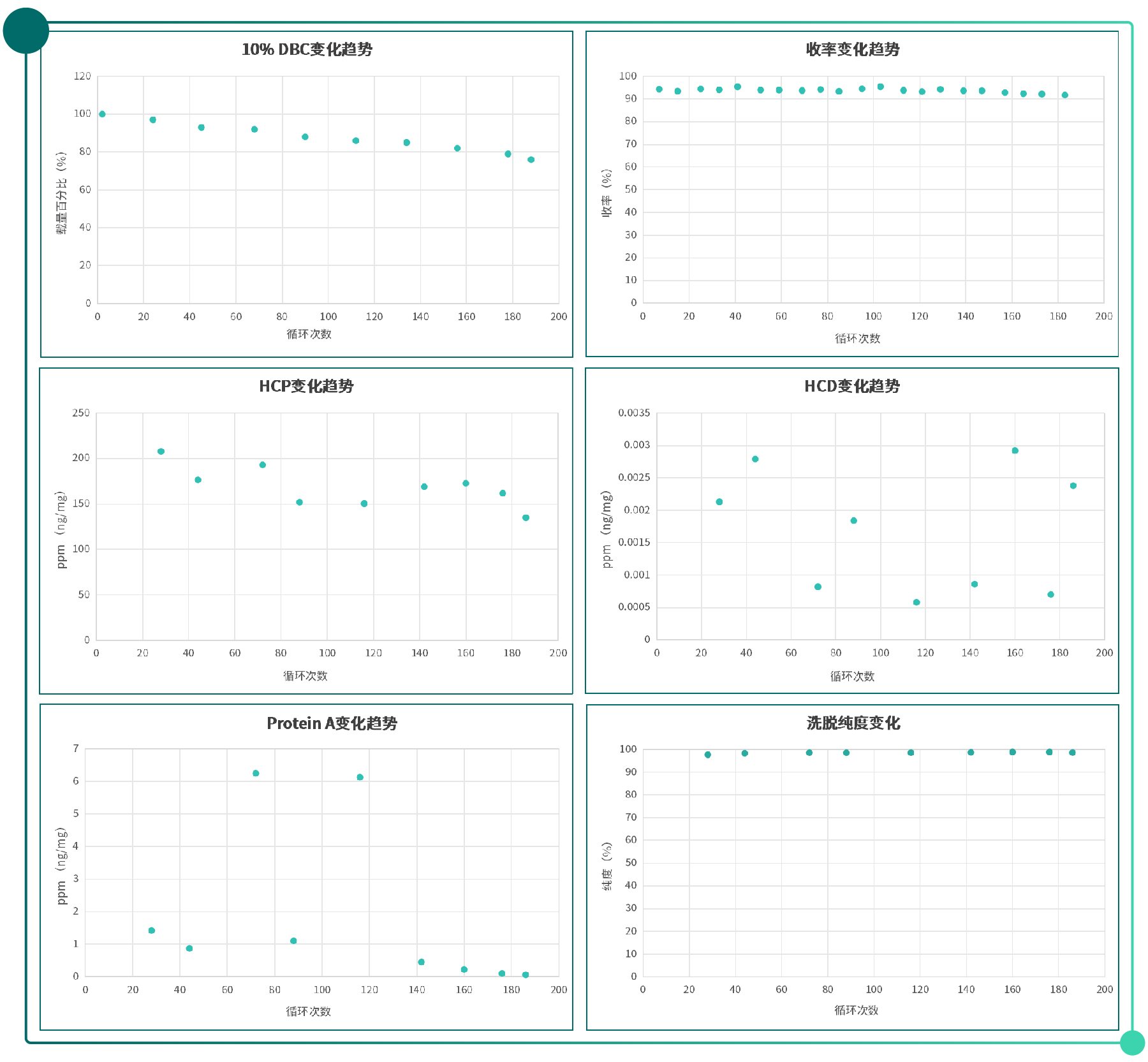 Fig.1 Novo-A Diamond 寿命研究各项数据检测结果图谱
Fig.1 Novo-A Diamond 寿命研究各项数据检测结果图谱总结
层析填料作为生物制药下游纯化工艺中至关重要的原材料,其性能与生物药物的产品质量密切相关。通过填料寿命研究实验,不仅仅提高了生产工艺的可控性与经济性,也为商业化生产提供可靠保证。
参考资料
[1] 2020 版《中国药典》三部“人用重组单克隆抗体制品总论”.
[2] FDA “Guidance for Industry:Process Validation: General Principles and Practices”.
[3] FDA “Points to Consider in the Manufacture and Testing ofMonoclonal Antibody Products for Human Use”.
[4] EMA “Guideline on process validation for the manufacture of biotechnology-derived active substances and data to be provided in the regulatory submission”.
[5] EMA “CPMP Position Statement on DNA and Host Cell Proteins (HCP) Impurities, Routine Testing Versus Validation Studies,” CPMP/BWP/382/97.
[6] PDA Technical Report No.60-3: Process validation: A lifecycle approach Annex 2: biopharmaceutical drug substances manufacturing. Parenteral Drug Association: 2021.
关于博格隆
博格隆成立于 2008年,是一家专注于为分离纯化提供高质量层析介质的高新技术企业,是中国较早具备大规模生产分离纯化介质能力的企业之一。博格隆所提供的产品涵盖亲和层析、离子交换层析、凝胶过滤层析、疏水层析、多模式层析、反相层析等不同类型的纯化介质以及预装柱、层析空柱、细胞培养用微载体,同时提供分离纯化工艺开发服务及填料定制服务。这些产品和服务被广泛应用于抗体纯化、疫苗纯化、胰岛素纯化、质粒纯化、重组蛋白纯化等多个领域。
